Introducción a las membranas de intercambio catiónico
Las membranas de intercambio catiónico (CEM) se denominan frecuentemente membranas de intercambio de protones (PEM) porque a menudo se utilizan en reacciones químicas que generan protones. Los CEM se utilizan en diversas aplicaciones, desde membranas de intercambio de protones y pilas de combustible microbianas hasta la producción de cloro y soda cáustica. La membrana de intercambio catiónico (CEM) contiene grupos funcionales cargados negativamente (PO3-, COO– y C6H4O–) en la columna vertebral de la membrana, lo que permite el paso de los cationes. Hay muchos tipos de CEM que se han utilizado en la literatura, incluidos Nafion©, Fumatech, Aquivion, Xion Composite, poliestireno, lana de vidrio, divinilbenceno y muchos otros. Los grupos funcionales más comunes para los CEM son el ácido sulfónico, el ácido carboxílico y los grupos de ácido fosfónico, como se muestra en la Tabla 1. Los tres tipos de grupos funcionales pueden intercambiar protones de hidrógeno (H+).
Tabla 1. Grupos funcionales comunes para membranas de intercambio catiónico (CEM).

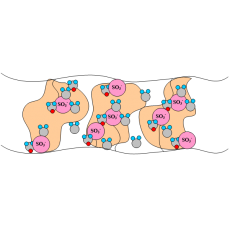
El CEM más común es Nafion©, un copolímero de poli(tetrafluoroetileno) y éter vinílico de fluoruro de polisulfonilo que tiene una alta conductividad protónica (0,2 S/cm) y es estable en entornos oxidativos y reductores. En esta membrana conductora de protones, los grupos de ácido sulfónico están unidos a una estructura polimérica basada en PTFE. El H+ salta del sitio SO3- al sitio SO3- a lo largo del material, donde el H+ emerge al otro lado de la membrana. La membrana debe permanecer hidratada para ser conductora de protones. Esto limita la temperatura de funcionamiento por debajo del punto de ebullición del agua y hace que la gestión del agua sea una cuestión clave cuando se utilizan membranas de ácido perfluorosulfónico. Las membranas Nafion© y otras membranas PFSA son estables frente al ataque químico de bases fuertes, ácidos oxidantes y reductores fuertes, H2O2, Cl2, H2 y O2 a temperaturas de hasta 125 ºC. La Figura 1 ilustra los sitios SO3- en la membrana Nafion©.

Figura 1. Ilustración pictórica de los grupos de ácidos sulfónicos en Nafion©
La estructura química de Nafion consiste en la fracción de ácido perfluorosulfónico unida a una cadena principal de fluorocarbono hidrófobo y demuestra una alta conductividad no solo para los protones de hidrógeno, sino también para varios tipos de cationes debido a la presencia de grupos sulfonato (SO3-) unidos, hidrófilos y cargados negativamente. . La Figura 2 ilustra la columna vertebral de fluorocarbono hidrofóbico de Nafion.

Figura 2. La estructura química de Nafion©.
Absorción de agua en Nafion
La membrana seca absorbe agua para solvatar los grupos ácidos. El contenido de agua inicial está fuertemente asociado con los sitios, y la adición de agua hace que el agua se una menos al polímero, lo que hace que las gotas de agua se agreguen. Los grupos de agua eventualmente crecen y forman interconexiones entre sí. Estas conexiones crean “canales de agua”, son transitorias y tienen hidrofobicidades comparables a las de la matriz. Una vía de transporte se forma cuando los grupos de agua están muy juntos y se vinculan. Este fenómeno de percolación ocurre cuando la relación mol H20/mol SO3- es alrededor de 2 (ver Figura 3). La siguiente etapa ocurre cuando se ha formado una red completa de canales de clúster. En la última etapa, los canales ahora están llenos de líquido y la absorción de la membrana ha aumentado sin cambio en el potencial químico del agua. Este fenómeno se conoce como la paradoja de Schroeder. En la Figura 3 se muestra una ilustración de la absorción de agua de la membrana Nafion©.

Figura 3. Ilustración pictórica de la captación de agua de Nafion©
La paradoja de Schroeder es un fenómeno observado que debe tenerse en cuenta cuando la membrana no está completamente hidratada ni deshidratada. Dependiendo del sistema, se puede suponer que la membrana está completamente hidratada o sólo llena de vapor; sin embargo, en realidad, el contenido de agua es dinámico. Nafion© exhibe una isoterma de absorción de agua como se muestra en la Figura 4.

Figura 4. Isoterma de absorción de agua a 25˚C que muestra el efecto de la paradoja de Schroder.
Comprender el contenido de agua en la membrana es importante porque la conductividad iónica es función del contenido de agua. Dos procesos de transporte que ocurren en la membrana polimérica son la difusión y el arrastre electroosmótico:
1. El arrastre electroosmótico ocurre cuando los protones de hidrógeno viajan a través de la membrana polimérica desde el ánodo al cátodo y transportan moléculas de agua con ellos. El número promedio de moléculas de agua «arrastradas» por un solo protón se llama coeficiente de arrastre electroosmótico.
2. La retrodifusión ocurre cuando el gradiente de concentración en el cátodo impulsa la difusión de agua a través de la membrana.
La acumulación de agua en el cátodo se produce tanto por el arrastre electroosmótico como por la producción de agua en el cátodo. El agua en el cátodo puede transportarse al canal de flujo a través del soporte de difusión de gas, evaporarse a través de calentadores o difundirse a través de la membrana hacia el ánodo.
La conductividad se puede aumentar mediante un equilibrio óptimo entre temperatura y agua, electrolitos o membranas más delgadas o materiales conductores de iones avanzados. Uno de los métodos más eficaces para aumentar la conductividad es utilizar una capa de electrolito más delgada (o membranas más delgadas) para que los iones tengan menos distancia que recorrer a través de la membrana para llegar al otro lado. Las membranas más delgadas también son ventajosas porque mantienen el electrodo del ánodo saturado mediante la difusión «inversa» de agua desde el cátodo. La cantidad de agua en la membrana debe equilibrar las ecuaciones de transporte de masa con los protones y el agua moviéndose a las velocidades necesarias.
Limitaciones
También existen varias desventajas de Nafion y otras membranas de ácido perfluorosulfónico, como el costo del material, los requisitos de la estructura de soporte y las limitaciones relacionadas con la temperatura. Para muchos sistemas basados en CEM, la eficiencia aumenta a temperaturas más altas, pero surgen problemas como la deshidratación de la membrana, la reducción de la conductividad iónica, la disminución de la afinidad por el agua, la pérdida de resistencia mecánica debido al ablandamiento de la columna vertebral del polímero y el aumento de las pérdidas parásitas debido a la alta permeabilidad del combustible. Empeorar. Nafion no es adecuado para pH neutro o soluciones que contengan especies catiónicas como Na+, K+ y NH4+. Estas especies son más permeables a través de la membrana que el H+; por lo tanto, este proceso provoca un aumento del pH en la cámara catódica.
Debido a las limitaciones de Nafion, se están investigando muchas otras membranas de intercambio catiónico. Las membranas alternativas a los hidrocarburos pueden proporcionar algunas ventajas sobre las membranas PFSA, como el costo, la disponibilidad comercial y la alta absorción de agua en un amplio rango de temperaturas, con el agua absorbida restringida a los grupos polares de las cadenas de polímeros. Las categorías de membranas que se están investigando actualmente incluyen: (1) perfluoradas, (2) parcialmente fluoradas, (3) no fluoradas (incluidos los hidrocarburos), (4) compuestos no fluorados (incluidos los hidrocarburos) y (5) otras. Ultrex se selecciona habitualmente como alternativa a los CEM debido a su alta estabilidad mecánica y asequibilidad. Un tipo comúnmente empleado es Ultrex CMI 7000, una membrana de polímero de ácido fuerte con un gel de poliestireno y una estructura reticulada de divinilbenceno con numerosos grupos de ácido sulfónico. Zirfon y Hyflon son otros CEM alternativos. Zirfon consta de un 85% en peso de un polvo de ZrO2 hidrófilo y un 15% en peso de polisulfona. Sin embargo, Zirfon tiene una mayor permeabilidad al oxígeno en comparación con Nafion, lo que puede ser perjudicial para ciertas reacciones anódicas. La mayoría de las membranas tienen temperaturas de degradación que oscilan entre 250 y 500 ºC, absorción de agua de 2,5 a 27,5 H2O/SO3H y conductancia de 10 mS/cm a 10 S/cm.
Resumen
La membrana de intercambio catiónico (CEM) debe ser un buen conductor de protones, químicamente estable y capaz de soportar las temperaturas y fuerzas de compresión del sistema operativo. Dependiendo del sistema, las propiedades de estabilidad y transporte de iones y agua deben considerarse simultáneamente. Hay muchas opciones de materiales CEM y la decisión con respecto a cada elección depende de muchos factores, incluidos, lo más importante, el costo y las capacidades de fabricación en masa.

